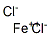
CAS号:7758-94-3
|
英文名称:Ferrous chloride
分子式
分子量
EINECS号
MDL
Smiles
InChIKey
氯化亚铁化学百科
基本信息
| 中文名称 | Iron(II) chloride |
| 英文名称 | Iron(II) chloride |
| CAS号 | 7758-94-3 |
| 分子式 | Cl2Fe |
| 分子量 | 126.751 |
| EINECS号 | 231-843-4 |
物化性质
| 熔点 | 677 °C (lit.) |
| 沸点 | 1023°C |
| 密度 | 3.16 g/mL at 25 °C (lit.) |
| 蒸气压 | 0Pa at 20℃ |
| 闪点 | 1023°C |
| 溶解度 | 可溶于水中 |
| 形态 | 珠状 |
| 颜色 | 米白色 |
| 比重 | 3.162 |
| 水溶解性 | Soluble in water, alcohol and acetone. Slightly soluble in benzene. Insoluble in ether. |
| 晶体结构 | CdCl2 type |
| 敏感性 | Hygroscopic |
| 默克索引编号 | 14,4043 |
| 暴露限值 | ACGIH: TWA 1 mg/m3NIOSH: TWA 1 mg/m3 |
安全信息
| 危险品标志 | C |
| 危险类别码 | 22-34 |
| 安全说明 | 26-36/37/39-45 |
| 危险品运输编号 | UN 3260 8/PG 3 |
| WGK Germany | 1 |
| RTECS号 | NO5400000 |
| TSCA | Yes |
| 海关编码 | 2827392000 |
| 危险等级 | 8 |
| 包装类别 | III |
| 毒害物质数据 | 7758-94-3(Hazardous Substances Data) |
生产及用途
氯化亚铁,化学式FeCl2。分子量 126.75。具有CdCl2型结构的白色菱状晶体。熔点672℃, 沸点1030℃,相对密度3.16225。在700℃的氯化氢气流中升华而得的白色晶体吸湿性极强。其二水合物为略呈淡绿色的无色单斜系晶体,相对密度2.358,在空气中易氧化,150~160℃时分解生成一水合物,220℃时失去全部结晶水。其四水合物为蓝绿色单斜系晶体,有吸湿性,相对密度1.93。极易溶于水与乙醇,溶于丙酮,稍溶于苯,不溶于乙醚。在潮湿空气中极易氧化。氯化亚铁可广泛用作还原剂,也用于染色中作媒染剂,还用于医药制剂及冶金工业中。将铁在干燥氯化氢气流中温度控制在500℃以下加热,或在300~350℃用干燥氢气还原无水三氯化铁而得。以三氯化铁为原料,与氯化苯在125℃下加热30min。用水吸收生成的氯化氢。继续在 130~139℃加热2h。则沉淀由黑变棕。粘度降低,在隔绝空气条件下滤取固体,用氯仿和苯洗涤,可制得氯化亚铁。不同温度(℃)时每100毫升水中的溶解克数:
49.7g/0℃;59g/10℃;62.5g/20℃;66.7g/30℃;70g/40℃
78.3g/60℃;88.7g/80℃;92.3g/90℃;94.9g/100℃

和氯反应,定量地生成氯化铁。氯化亚铁与水蒸气则发生如下反应:(1) 3FeCl2+4H2O→Fe3O4+6HCl+H2 (2) 6FeCl2+3H2O→4FeCl3+Fe2O3+3H2。
当释放氯化氢的速度减慢,氯化铁变成白色结晶时,表示反应完毕,停止加热,并在弱氢气流中使管中产物降至室温。将反应管封闭存放,然后迅速装人包装容器,制得无水氯化亚铁,其反应方程式:2FeCl3+H2→2FeC12+2HCl
49.7g/0℃;59g/10℃;62.5g/20℃;66.7g/30℃;70g/40℃
78.3g/60℃;88.7g/80℃;92.3g/90℃;94.9g/100℃
化学性质
常温下氯化亚铁为白色或灰绿色结晶。易吸湿。在空气中易被氧化而渐变成黄色。相对密度d4253.162。熔点677℃。沸点1023℃。熔化热43.01 kJ/mol,在氯化氢气流中约700℃升华。易溶于水、甲醇、乙醇,微溶于丙酮及苯,不溶于乙醚。
和氯反应,定量地生成氯化铁。氯化亚铁与水蒸气则发生如下反应:(1) 3FeCl2+4H2O→Fe3O4+6HCl+H2 (2) 6FeCl2+3H2O→4FeCl3+Fe2O3+3H2。
用途
用于冶金、医药制造。用作分析试剂、水处理净化剂、媒染剂、无铅汽油助剂和还原剂。生产方法
在一硬质玻璃管中迅速放人无水三氯化铁,自管的一端通人经干燥的氢气,充分置换除去管内的空气后,将反应管加热,管的另一端即有大量氯化氢排出,可用水吸收成稀盐酸。当释放氯化氢的速度减慢,氯化铁变成白色结晶时,表示反应完毕,停止加热,并在弱氢气流中使管中产物降至室温。将反应管封闭存放,然后迅速装人包装容器,制得无水氯化亚铁,其反应方程式:2FeCl3+H2→2FeC12+2HCl
类别
腐蚀物质毒性分级
高毒急性毒性
口服- 大鼠 LD50 450 毫克/ 公斤; 腹腔- 小鼠 LD50: 59 毫克/公斤可燃性危险特性
不可燃烧; 火场产生有毒含铁化物和氯化物烟雾储运特性
库房低温, 通风, 干燥; 与食品原料分开存放灭火剂
水, 二氧化碳, 干粉, 砂土职业标准
TWA 1 毫克(铁)/立方米; STEL 2 毫克(铁)/立方米上下游产品
相关产品
-
CAS号:7718-54-9
无水氯化镍(II)(99.99 +%-Ni) , (99.99+%-Ni) -
CAS号:141-01-5
富马酸亚铁(II) -
CAS号:7757-82-6
硫酸钠 , 用于分析 -
CAS号:584-08-7
碳酸钾 -
CAS号:1317-60-8
红色氧化铁(III)(赤铁矿) -
CAS号:1330-43-4
无水硼砂 -
CAS号:7720-78-7
硫酸亚铁 -
CAS号:7758-98-7
硫酸铜 -
CAS号:13463-43-9
一水硫酸亚铁 -
CAS号:7646-79-9
氯化亚钴 -
CAS号:7439-89-6
铁粉 -
CAS号:7487-88-9
硫酸镁 -
CAS号:497-19-8
纯碱 -
CAS号:7786-30-3
氯化镁


