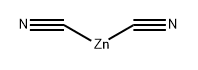
CAS号:557-21-1
|
英文名称:zinc,dicyanide
分子式
分子量
EINECS号
MDL
Smiles
InChIKey
氰化锌化学百科
基本信息
| 中文名称 | 氰化锌 |
| 英文名称 | zinc cyanide |
| CAS号 | 557-21-1 |
| 分子式 | C2N2Zn |
| 分子量 | 0 |
| EINECS号 | 209-162-9 |
物化性质
| 熔点 | 800 °C |
| 密度 | 1,85 g/cm3 |
| 蒸气压 | 0Pa at 25℃ |
| LogP | -2.31 at 25℃ |
| 溶解度 | 碱性溶液(微溶) |
| 形态 | 粉末 |
| 颜色 | 白色至类白色 |
| 水溶解性 | Soluble in alkalies, potassium cyanide and ammonia. Insoluble in water and most solvents. |
| 敏感性 | Hygroscopic |
| 默克索引编号 | 14,10135 |
| BRN | 4124366 |
| 暴露限值 | NIOSH: IDLH 25 mg/m3 |
| 稳定性 | 湿气敏感 |
安全信息
| 危险品标志 | N-T+,N,T+ |
| 危险类别码 | 50/53-32-26/27/28 |
| 安全说明 | 7-61-60-45-29-28A-28 |
| 危险品运输编号 | 1713 |
| WGK Germany | 3 |
| RTECS号 | ZH1575000 |
| TSCA | Yes |
| 海关编码 | 28371990 |
| 危险等级 | 6.1 |
| 包装类别 | I |
| 毒害物质数据 | 557-21-1(Hazardous Substances Data) |
生产及用途
氰化锌,化学式Zn(CN)2。分子量 117.41。白色粉末或斜方系有光泽柱状晶体。有毒!相对密度1.852。800℃时分解。不溶于水(微溶于热水)、乙醇和乙醚,溶于氰化物溶液形成Zn(CN)42-络离子,也溶于碱液和氨水。吸收潮湿空气中的二氧化碳,生成碳酸锌而放出极毒的氰化氢气体。应保存在密闭容器中。制法:由锌盐和适量的氰化钠溶液反应而得。用途:主要用于电镀、医药 (消毒剂、驱虫药)、农药等方面。
5.8×10-2/20℃参见氰化钾。
将经沉降的氯化锌清液放入反应器内,加人氰化钠溶液使反应生成氰化锌沉淀。为防止生成的氰化锌溶于过量的氰化钠溶液而形成Na2Zn(CN)4复盐溶液,故氰化钠溶液的加人量应加以控制。沉淀用水漂洗除氯化钠,然后经离心分离、干燥,制得氰化锌成品。其
2NaCN+ZnC12→Zn(CN)2+2NaCl
氰化锌蒸气对吸道有刺激性,吸入后可引起氰化物中毒,出现头痛、乏力、呼吸困难、皮肤粘膜呈鲜红色、抽搐、昏迷等。
高浓度吸入氰化锌后立即引起呼吸心跳停止而死亡。可引起皮肤和眼灼伤。口服可致死。
5.8×10-2/20℃参见氰化钾。
化学性质
氰化锌,白色有光泽柱状结晶或无定形块状固体或粉末。不溶于冷水、氢氰酸、乙醇和乙醚,微溶于热水,溶于液碱、氨水、冰醋酸锌溶液中,溶于氰化钠、氰化钾溶液形成复盐。不溶于有机酸中,能溶于稀的无机酸并分解释放出氰化氢,溶于碱金属氰化物、氢氧化物和氨水形成配离子。会吸收潮湿空气中的二氧化碳,生成碳酸锌而释出氢氰酸。氰化锌有剧毒。食入后能引起氰化物中毒,口服可致死。用途
用于电镀、有机合成、医药和农药的制造生产方法
合成法氰化钠用水溶解,加入氯化钡以除去碳酸钠杂质;氯化锌用水溶解,如溶液混浊,需加人盐酸,调Ph 5~6使溶液中ZnO转换成ZnCl2。将经沉降的氯化锌清液放入反应器内,加人氰化钠溶液使反应生成氰化锌沉淀。为防止生成的氰化锌溶于过量的氰化钠溶液而形成Na2Zn(CN)4复盐溶液,故氰化钠溶液的加人量应加以控制。沉淀用水漂洗除氯化钠,然后经离心分离、干燥,制得氰化锌成品。其
2NaCN+ZnC12→Zn(CN)2+2NaCl
类别
农药毒性分级
高毒急性毒性
腹腔- 大鼠 LDL0: 100 毫克/ 公斤可燃性危险特性
不可燃物质; 遇水、酸放出有毒易燃氰化氢气体储运特性
库房通风低温干燥; 与碱、酸类、食品添加剂分开存放上下游产品
上游产品共计:6个
-
CAS号:7733-02-0
硫酸锌 -
CAS号:10361-37-2
氯化钡 -
CAS号:7446-20-0
七水硫酸锌 -
CAS号:7733-02-0
硫酸锌 -
CAS号:10361-37-2
氯化钡 -
CAS号:7446-20-0
七水硫酸锌
下游产品共计:18个
-
CAS号:951624-83-2
5-(三氟甲基)烟腈 -
CAS号:34136-59-9
2-乙基苯甲腈 -
CAS号:344327-11-3
7-氮杂吲哚-4-甲腈 -
CAS号:327056-62-2
2-氰基-5-氟吡啶 -
CAS号:873-62-1
3-羟基苯腈 -
CAS号:123-08-0
4-羟基苯甲醛 , 用于合成 -
CAS号:403-54-3
3-氟苯甲腈 -
CAS号:24964-64-5
3-氰基苯甲醛 -
CAS号:35066-32-1
3-氰基-4-甲基苯甲酸甲酯 -
CAS号:951624-83-2
5-(三氟甲基)烟腈 -
CAS号:34136-59-9
2-乙基苯甲腈 -
CAS号:344327-11-3
7-氮杂吲哚-4-甲腈 -
CAS号:327056-62-2
2-氰基-5-氟吡啶 -
CAS号:873-62-1
3-羟基苯腈 -
CAS号:123-08-0
4-羟基苯甲醛 , 用于合成 -
CAS号:403-54-3
3-氟苯甲腈 -
CAS号:24964-64-5
3-氰基苯甲醛 -
CAS号:35066-32-1
3-氰基-4-甲基苯甲酸甲酯
相关产品
-
CAS号:557-21-1
氰化锌 -
CAS号:557-21-1
氰化锌 -
CAS号:14049-79-7
钴氰化锌 -
CAS号:557-21-1
氰化锌 -
CAS号:544-92-3
氰化亚铜 -
CAS号:14320-04-8
酞菁锌 -
CAS号:14763-77-0
氰化铜 -
CAS号:557-21-1
氰化锌 -
CAS号:87-90-1
三氯异氰脲酸 -
CAS号:544-97-8
二甲基锌 -
CAS号:20427-58-1
氢氧化锌 -
CAS号:506-64-9
氰化银 -
CAS号:7446-20-0
七水硫酸锌 -
CAS号:2893-78-9
二氯异氰尿酸钠 -
CAS号:557-21-1
氰化锌 -
CAS号:557-21-1
氰化锌 -
CAS号:14049-79-7
钴氰化锌 -
CAS号:557-21-1
氰化锌 -
CAS号:544-92-3
氰化亚铜 -
CAS号:14320-04-8
酞菁锌 -
CAS号:14763-77-0
氰化铜 -
CAS号:557-21-1
氰化锌 -
CAS号:87-90-1
三氯异氰脲酸 -
CAS号:544-97-8
二甲基锌 -
CAS号:20427-58-1
氢氧化锌 -
CAS号:506-64-9
氰化银 -
CAS号:7446-20-0
七水硫酸锌 -
CAS号:2893-78-9
二氯异氰尿酸钠
产品供应商

