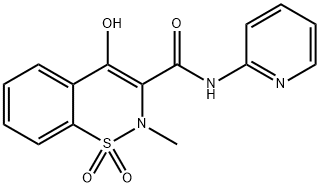
| 中文名称 | 吡罗昔康 |
| 英文名称 | Piroxicam |
| CAS号 | 36322-90-4 |
| 分子式 | C15H13N3O4S |
| 分子量 | 331.35 |
| EINECS号 | 252-974-3 |
| 熔点 | 198-200°C |
| 密度 | 1.3664 (rough estimate) |
| 折射率 | 1.6320 (estimate) |
| 溶解度 | 几乎不溶于水,溶于二氯甲烷,微溶于无水乙醇。 |
| 形态 | 固体 |
| 酸度系数(pKa) | 6.3 (2:1 dioxane-water) |
| 颜色 | 白色至浅黄色至浅橙色 |
| 水溶解性 | Soluble in water, ethanol, chloroform, ethyl acetate. |
| 最大波长(λmax) | 358nm(H2O)(lit.) |
| 默克索引编号 | 14,7506 |
| 危险品标志 | Xn,F,T |
| 危险类别码 | 22-25 |
| 安全说明 | 26-36 |
| 危险品运输编号 | UN 2811 |
| WGK Germany | 3 |
| RTECS号 | DL0705000 |
| 海关编码 | 29349990 |
| 危险等级 | 6.1(b) |
| 包装类别 | III |
| 毒性 | LD50 orally in mice: 360 mg/kg (Wiseman) |
吡罗昔康为苯并噻嗪类非甾体类长效抗炎药,对体内PG的合成酶有强大的抑制作用,并有抑制白细胞向炎症区域移动和溶酶体酶向外释放的作用,故具有很强的解热、镇痛、抗炎、抗风湿作用及一定的消肿作用。主要用于肌肉、骨骼和关节等疾病,如关节强硬性脊椎炎、骨关节炎、类风湿性关节炎和急性痛风。

吡罗昔康为类白色或微黄绿色结晶性粉末,无臭,无味。几乎不溶于水,微溶于乙醇或乙醚,易溶于氯仿,略溶于丙酮,溶于酸液。
吡罗昔康为长效非甾体类抗炎镇痛解热药,具有镇痛、抗炎及解热作用。本品通过抑制环氧酶,使组织局部前列腺素的合成减少及抑制白细胞的趋化性和溶酶体酶的释放而发挥药理作用。口服吸收迅速而完全,食物可降低吸收速度,但不影响吸收总量。Tmax3~5h。T1/2为30~86h,PPB大于90%,肾功能不全患者T1/2延长,主要经肝脏代谢。由于T1/2较长,一次给药即可维持24h的血药浓度相对稳定,多次给药易致蓄积。血药有效浓度为1.5~2μg/ml。血药稳定浓度在开始治疗后7~12d方能达到。66%自肾脏排泄,33%自粪便排泄,内有<5%为原形物。
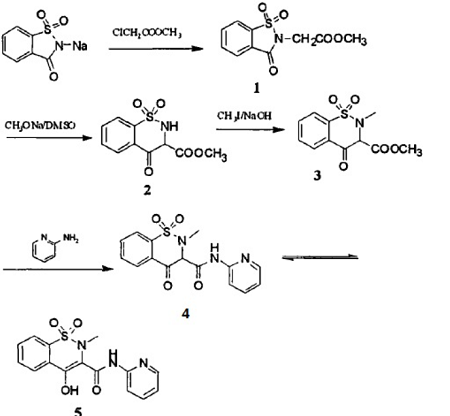
吡罗昔康的制备方法:
(1)3-氧代-1,2-苯并异噻唑啉-2-乙酸甲酯-1,1二氧化物(1)
在装有搅拌器、温度计、冷凝管500mL的反应瓶中,加入150mL的常压脱水,完毕降室温,加入二水糖精钠85g升温负压脱水真空度(-0.095~0.098MPa),脱毕升温在110℃滴加氯乙酸乙酯60g,约60min滴毕,在110~115℃维持反应4h,再减压操作蒸出DMF,温度降至85℃左右备用。
(2)3,4-二氧-4-氧化-2H-1,2-苯并噻嗪-3-羧酸甲酯-1,1-二氧化物
在上述85℃产物中加28%的甲醇钠330g搅拌下逐渐升温,温度在82℃时反应液出现黄色并逐渐变稠,减压蒸出乙醇,降温到30℃备用。
(3)2-甲基-3,4-二氧-4-氧化-2H-1,2-苯并噻嗪-3-羧酸甲酯-1,1-二氧化物
将5℃的水倒人上述产物中搅拌降温至12℃以下,用20%的HCl调节pH至8~9,降温至8℃时滴加90gDMSO,约60min滴毕,在12~15℃搅拌5h,反应完用20%的HCl调pH至5,抽滤。干燥的白色针状晶体90g。
(4)吡罗昔康粗品的制备
在装有分馏柱的2000mL反应瓶中,加入1600mL的二甲苯,2=氨基吡啶12g,在搅拌下加(3),升,110~117℃时反应90min,二甲苯缓缓蒸出,温度在136~142℃反应8h,后继续反应18h,二甲苯的量蒸出约600g时降温至10℃析出固体过滤,用少量乙醇洗涤,干燥得89g(4)。
(5)吡罗昔康的制备
将89g的(4)用6%的NaOH180mL与180mL的乙醇混合液脱色溶解过滤,滤液用20%的HCl调pH值至2~3,过滤,水洗中性,在用少量乙醇洗涤,干燥得微黄白色粉末状晶体83.7g。
吡罗昔康适用于类风湿性关节炎、骨关节炎、强直性脊椎炎及急性痛风性关节炎的症状。
口服:每次20mg,每日1次。用于痛风,每次40mg,每日1次或分次服用,连用4~6日,不宜长期服用。成人关节炎:po,20mg,qd,饭后服;急性痛风:po,40mg,qd,连用4~6d。老年患者可能需降低剂量,且需要限制用药时间。常见胃肠道反应如恶心、呕吐、胃部不适、腹痛、腹泻、便秘等,发生率约20%。服药量大于一日20mg时胃溃疡发生率明显增高,有的合并出血,甚至穿孔。中性粒细胞减少、嗜酸粒细胞增多、血小板减少、血尿素氮增高、头晕、眩晕、耳鸣、头痛、全身无力、水肿,皮疹或瘙痒等,发生率1%~3%。本品治疗关节炎时的镇痛、消肿等疗效与吲哚美辛、阿司匹林、萘普生相似。Marcucci等随机治疗20例急性牙周炎患者,单剂量口服喜来通20mg或甲氯芬那酸100mg,结果发现甲氯芬那酸起效快,镇痛效果与喜来通相当,但是单剂量喜来通的镇痛作用时间明显比甲氯芬那酸长。1.对服用乙酰水杨酸或其他非甾体抗炎药引起哮喘、鼻炎的患者,对本品过敏者,消化性溃疡、慢性胃病患者,孕妇、哺乳期妇女和儿童禁用本品。
2.有胃肠道出血或溃疡病史、肾功能不全、心血管疾病患者慎用。
3.有凝血机制或血小板功能障碍、哮喘、心功能不全或高血压、肾功能不全的患者及老年人慎用。
4.长期用药者应定期复查肝、肾功能及血象。
5.可抑制血小板聚集,作用比阿司匹林弱,但可持续到停药后2周,术前和术后应停用。
6.与双香豆素等抗凝药同用时,后者效应增强,出血倾向显著,用量宜调整。
7.与阿司匹林同用时,本品的血药浓度可下降到一般浓度的80%,同时胃肠道溃疡形成和出血倾向的危险性增加。
8.本品不宜长期服用,因可引起胃溃疡及大出血。[1]宋文阁,王春亭,傅志俭等主编.实用临床疼痛学.郑州:河南科学技术出版社.2008.第139页.
[2]周文,周序斌,韩文修主编.最新药物手册.济南:山东科学技术出版社.2005.第135-136页.
[3]实用药物手册.济南:山东科学技术出版社.1999.第484-485页.
[4]周萍.吡罗昔康贴剂的研制[J].中国药学杂志,2001,(03):28-29.
[5]余超英.吡罗昔康栓剂的制备方法[J].黑龙江医药,2008,(03):59-60.
[6]董平.吡罗昔康两种透皮给药制剂的研究[D].复旦大学,2010.
[7]付金广.吡罗昔康工艺的改进[J].山东化工,2013,42(09):19-20.
-
CAS号:5221-37-4
2-氯-N-吡啶-2-基乙酰胺 -
CAS号:64-17-5
乙醇 -
CAS号:65897-46-3
吡罗昔康杂质 B -
CAS号:15448-99-4
N-甲基糖精 -
CAS号:124-41-4
甲醇钠 -
CAS号:128-44-9
糖精钠 -
CAS号:1310-73-2
氢氧化钠 -
CAS号:504-29-0
2-氨基吡啶 -
CAS号:118854-48-1
4-羟基-2-甲基-2-甲基-2H-1,2-苯并噻嗪-3-羧酸异丙酯1,1-二氧化物(吡罗昔康杂质L) -
CAS号:74-88-4
甲基碘 -
CAS号:91-33-8
苄噻嗪 -
CAS号:105-39-5
氯乙酸乙酯 -
CAS号:5221-37-4
2-氯-N-吡啶-2-基乙酰胺 -
CAS号:64-17-5
乙醇 -
CAS号:65897-46-3
吡罗昔康杂质 B -
CAS号:15448-99-4
N-甲基糖精 -
CAS号:124-41-4
甲醇钠 -
CAS号:128-44-9
糖精钠 -
CAS号:1310-73-2
氢氧化钠 -
CAS号:504-29-0
2-氨基吡啶 -
CAS号:118854-48-1
4-羟基-2-甲基-2-甲基-2H-1,2-苯并噻嗪-3-羧酸异丙酯1,1-二氧化物(吡罗昔康杂质L) -
CAS号:74-88-4
甲基碘 -
CAS号:91-33-8
苄噻嗪 -
CAS号:105-39-5
氯乙酸乙酯
-
CAS号:500008-45-7
氯虫苯甲酰胺 -
CAS号:99-76-3
4-羟基苯甲酸甲酯 , 用于合成 -
CAS号:90101-16-9
屈昔康 -
CAS号:99464-64-9
安吡昔康 -
CAS号:75-05-8
乙腈 , 99.9% , 超干溶剂, 水含量≤30 ppm, J&Kseal瓶 -
CAS号:59804-37-4
替诺昔康 -
CAS号:71125-38-7
美洛昔康 , 一种选择性COX抑制剂 -
CAS号:68-12-2
N,N-二甲基甲酰胺 , 99.8% , 超干溶剂, J&KSeal瓶, 水:≤30 ppm, 带分子筛 -
CAS号:8004-87-3
甲基紫 -
CAS号:143390-89-0
醚菌酯 -
CAS号:109-00-2
3-羟基吡啶 -
CAS号:70374-39-9
氯诺昔康 -
CAS号:67-56-1
甲醇 -
CAS号:1914-99-4
偶氮氯膦Ⅲ -
CAS号:75-12-7
甲酰胺 -
CAS号:500008-45-7
氯虫苯甲酰胺 -
CAS号:99-76-3
4-羟基苯甲酸甲酯 , 用于合成 -
CAS号:90101-16-9
屈昔康 -
CAS号:99464-64-9
安吡昔康 -
CAS号:75-05-8
乙腈 , 99.9% , 超干溶剂, 水含量≤30 ppm, J&Kseal瓶 -
CAS号:59804-37-4
替诺昔康 -
CAS号:71125-38-7
美洛昔康 , 一种选择性COX抑制剂 -
CAS号:68-12-2
N,N-二甲基甲酰胺 , 99.8% , 超干溶剂, J&KSeal瓶, 水:≤30 ppm, 带分子筛 -
CAS号:8004-87-3
甲基紫 -
CAS号:143390-89-0
醚菌酯 -
CAS号:109-00-2
3-羟基吡啶 -
CAS号:70374-39-9
氯诺昔康 -
CAS号:67-56-1
甲醇 -
CAS号:1914-99-4
偶氮氯膦Ⅲ -
CAS号:75-12-7
甲酰胺


