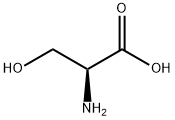
| 中文名称 | DL-丝氨酸 |
| 英文名称 | DL-Serine |
| CAS号 | 302-84-1 |
| 分子式 | C3H7NO3 |
| 分子量 | 105.09 |
| EINECS号 | 206-130-6 |
| 熔点 | 240 °C (dec.) (lit.) |
| 沸点 | 197.09°C (rough estimate) |
| 密度 | 1.53 |
| 折射率 | 1.4368 (estimate) |
| LogP | -3.460 |
| 溶解度 | 在水中可溶 |
| 形态 | 结晶粉末 |
| 酸度系数(pKa) | 2.19(at 25℃) |
| 颜色 | 白色 |
| 气味 (Odor) | 无味 |
| 水溶解性 | 50.23 g/L (25 ºC) |
| 默克索引编号 | 14,8460 |
| BRN | 1721402 |
| 危险品标志 | Xi |
| 危险类别码 | 36/37/38 |
| 安全说明 | 24/25-36-26 |
| WGK Germany | 3 |
| RTECS号 | VT8100000 |
| TSCA | Yes |
| 海关编码 | 29225000 |
DL-丝氨酸又称2-氨基-3-羟基丙酸、β-羟基丙氨酸、羟基氨基丙酸,一种含有羟基的脂肪族中性氨基酸,有极性但不带电荷,属人体非必需氨基酸,在丝胶蛋白和丝蛋白中含量丰富,它可由甘氨酸转甲基形成,也可脱氨转变为丙酮酸或羟基丙酮酸,也是体内合成胆碱和半胱氨酸的重要原料。
1865年首次从丝胶的硫酸水解溶液中分离出来。有左旋体和外消旋体。左旋体从水中结晶制得者为六方晶系片状或棱柱状白色晶体或结晶性粉末。无嗅。味甜。相对分子质量105.09。228℃分解。真空条件下150℃升华。旋光度-6.83°(10%水溶液)。难溶于有机溶剂,不溶于无水乙醇和乙醚,溶于酸和碱,易溶于水25.4(10℃)、38(20℃)、48.5(30℃)、60.5(40℃)、 72.0(50℃)、83.0(60℃)及甲酸。用于生物化学和营养学研究。也用作为合成环丝氨酸的原料。分布于多种蛋白质中,特别是蚕丝蛋白质中。在海洋浮游生物的氨基酸组成中含量居中。并以游离和结合状态存在于海水、颗粒物和海洋沉积物中,可由蛋白质水解物分离精制而得。也可由α-溴 -β-甲氧基丙酸经胺化及脱甲基制取。
外消旋体从水中结晶者为单斜晶系叶片状白色晶体。相对密度1.537。246℃分解。高真空时150℃升华。溶于水 (g/l)22.04(0℃)、50.23(50℃)、192(75℃)、322 (100℃),不溶于无水乙醇、乙醚、苯和醋酸。与过氧化氢和硫酸亚铁作用生成羟乙醛,与氯化铁溶液作用呈现红色,与盐酸作用得盐酸盐,在脱水剂存在下,与醇作用生成丝氨酸酯。
主要用途:
1,除了作为合成蛋白质的原料和在合成嘌呤、胸腺嘧啶、甲硫氨酸和胆碱等重要物质中提供碳架外,一些酶的活性中心组成以及植物体内乙醇酸途径的运行均需它参加。
2,因有特殊的润湿性,故用作化妆品添加剂,用于膏霜(保湿剂)维持角质层的水分,保持皮肤的柔软性;食品添加剂,用作营养增补剂;医药原料及输液。
丝氨酸可以从大豆、酿酒发酵剂、乳制品、鸡蛋、鱼、乳白蛋白、豆荚、肉、坚果、海鲜、种子、大豆、乳清和全麦中获取。
DL-丝氨酸可通过一下方式制取:
1,萃取法。将含丝氨酸较多的蛋白进行水解,然后用离子交换树脂萃取精制。
2,以乙醇醛、氢氰酸和氨为原料,进行合成,制得氨基腈后,再水解,可制得。
3,发酵法。以葡萄糖为碳源,以甘氨酸为前体,采用嗜甘氨酸棒杆菌或微白八叠球菌等经发酵可制得。或以甲醇为碳源,采用假单胞菌3ab或假单胞菌MS31等经发酵可制取。
4,以丙烯腈为原料,经氯化,生成α,β-二氯丙腈,再氨化,生成α-氯-β-氨基丙腈,然后在碱溶液中生成氮丙啶-2-羧酸钠,经强酸性阳离子交换树脂,可制得DL-丝氨酸。
5,以氯乙醛为原料,用亚硫酸氢钠还原再与碱作用,生成α-氨基-β-氯乙烷磺酸钠,进一步用氰化钠氰化,制得α-氨基-β-氯丙腈,最后再按丙烯腈法制得。
6,α-异氰乙酰胺与甲醛反应,生成喹唑啉中间体,直接水解制得。
7,电解还原法。先将丙酰胺酸乙酯氧化为相应的肟,然后以氯化锂为支持电解质,两极分别为铅及铂,进行电解还原,可制得。
8,以乙醇胺为原料,在催化剂钨酸钠作用下与过氧化氢进行氧化,再经氰化钠氰化,生成氨基腈,最后在盐酸中水解,可制得DL-丝氨酸。
蚕体内大量增加的丙氨酸和甘氨酸,可以在转氨酶的参与下,将氨基分别从另一种氨基酸(谷氨酸或天门冬氨酸)移转到丙酮酸或乙醛酸生成。丙氨酸可在谷天转氨酶、草酰乙酸脱羧酶及谷丙转氨酶的相继作用下生成。也可通过鸟氨酸转氨酶生成(许廷森等,1980)。丝腺组织能以酮丙二酸为氨基受体,进行转氨作用生成氨基丙二酸,然后在氨基丙二酸脱羧酶的催化下,生成甘氨酸(邹柏祥等,1979)。甘氨酸可与丝氨酸互相转变,葡萄糖通过3—磷酸羟基丙酮酸也能生成丝氨酸,丝氨酸经丙酮酸而生成丙氨酸。酪氨酸可由苯丙氨酸生成,胱氨酸可由蛋氨酸转变生成但不能相反转变,所以苯丙氨酸、蛋氨酸均为必需氨基酸。当饲料中富有酪氨酸和胱氨酸时,可以减少苯丙氨酸和蛋氨酸的需要量。取0.1%试样液5ml,加lml水合茚三酮试液(TS-250),应呈现蓝紫色或紫色。精确称取试样约200mg,溶于3ml甲酸和50ml冰醋酸中。用0.1mol/L高氯酸的冰醋酸液滴定,终点用电位计测定。同时作空白试验并作必要的校正。每Ml 0.1mol/L高氯酸相当于DL-丝氨酸(C3H7NO3)10.5lmg。
-
CAS号:4726-84-5
2-氨基丙酰胺 -
CAS号:598-42-5
羟基乙酰胺 -
CAS号:113-21-3
乳酸盐 -
CAS号:56-40-6
甘氨酸 , 用于分析 -
CAS号:4726-84-5
2-氨基丙酰胺 -
CAS号:598-42-5
羟基乙酰胺 -
CAS号:113-21-3
乳酸盐 -
CAS号:56-40-6
甘氨酸 , 用于分析
-
CAS号:312-84-5
D-丝氨酸 -
CAS号:2768-56-1
Cbz-DL-丝氨酸 -
CAS号:600-19-1
甘油酸 -
CAS号:212650-43-6
4-Boc-3-吗啉甲酸 -
CAS号:56-40-6
甘氨酸 , 用于分析 -
CAS号:56-45-1
L-丝氨酸 , 用于生化,[α] 20/ D:14.3°-16.0° -
CAS号:54-12-6
色氨酸 -
CAS号:56-89-3
L-胱氨酸 -
CAS号:53714-56-0
亮丙瑞林 -
CAS号:39978-59-1
丝氨酸乙酯 -
CAS号:312-84-5
D-丝氨酸 -
CAS号:2768-56-1
Cbz-DL-丝氨酸 -
CAS号:600-19-1
甘油酸 -
CAS号:212650-43-6
4-Boc-3-吗啉甲酸 -
CAS号:56-40-6
甘氨酸 , 用于分析 -
CAS号:56-45-1
L-丝氨酸 , 用于生化,[α] 20/ D:14.3°-16.0° -
CAS号:54-12-6
色氨酸 -
CAS号:56-89-3
L-胱氨酸 -
CAS号:53714-56-0
亮丙瑞林 -
CAS号:39978-59-1
丝氨酸乙酯
-
CAS号:107-95-9
β-氨基丙酸 -
CAS号:312-84-5
D-丝氨酸 -
CAS号:79-33-4
L-(+)-乳酸 , 90% -
CAS号:501-97-3
对羟基苯丙酸 -
CAS号:672-15-1
L-高丝氨酸 -
CAS号:1068-90-2
乙酰氨基丙二酸二乙酯 -
CAS号:617-48-1
DL-苹果酸(标准品) -
CAS号:5437-67-2
硝基丙二酸二甲酯 -
CAS号:24830-94-2
D-别苏氨酸 -
CAS号:462-08-8
3-氨基吡啶 -
CAS号:56-40-6
甘氨酸 , 用于分析 -
CAS号:56-45-1
L-丝氨酸 , 用于生化,[α] 20/ D:14.3°-16.0° -
CAS号:1145-80-8
|N|-苄氧羰基-L-丝氨酸 -
CAS号:16798-45-1
苯氨基丙二酸二乙酯 -
CAS号:603-67-8
2-硝基丙二酸二乙酯 -
CAS号:6326-44-9
二乙基氨基甲肟 -
CAS号:68-41-7
D-环丝氨酸 -
CAS号:107-95-9
β-氨基丙酸 -
CAS号:312-84-5
D-丝氨酸 -
CAS号:79-33-4
L-(+)-乳酸 , 90% -
CAS号:501-97-3
对羟基苯丙酸 -
CAS号:672-15-1
L-高丝氨酸 -
CAS号:1068-90-2
乙酰氨基丙二酸二乙酯 -
CAS号:617-48-1
DL-苹果酸(标准品) -
CAS号:5437-67-2
硝基丙二酸二甲酯 -
CAS号:24830-94-2
D-别苏氨酸 -
CAS号:462-08-8
3-氨基吡啶 -
CAS号:56-40-6
甘氨酸 , 用于分析 -
CAS号:56-45-1
L-丝氨酸 , 用于生化,[α] 20/ D:14.3°-16.0° -
CAS号:1145-80-8
|N|-苄氧羰基-L-丝氨酸 -
CAS号:16798-45-1
苯氨基丙二酸二乙酯 -
CAS号:603-67-8
2-硝基丙二酸二乙酯 -
CAS号:6326-44-9
二乙基氨基甲肟 -
CAS号:68-41-7
D-环丝氨酸


