芳基醛/酮的直接、高选择性、高效且通用的还原胺化、醚化、酯化和膦化反应,二苯基氧磷显神通!
背景介绍
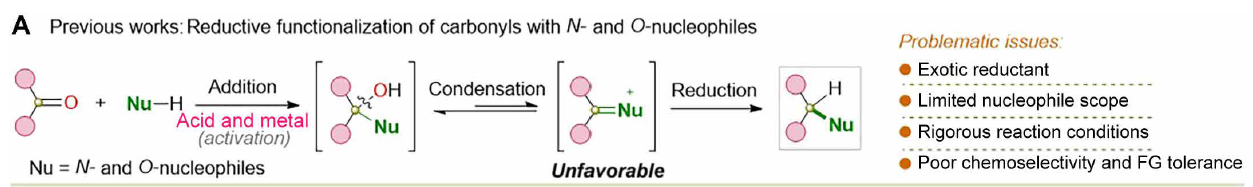
在制药工业中,至少有四分之一的C─N键形成是通过羰基还原胺化实现的。然而,羰基化合物的还原功能化在裂解和转化强C─O双键方面面临挑战。这些困难过程不可避免地需要借助奇特的还原剂、过渡金属催化剂和/或严格的反应条件,而在某些情况下,甚至需要将羰基预先转化为腙以实现后续功能化。
图片来源:Sci. Adv.
本期小编给大家介绍一种简单且极其通用的羰基还原功能化策略,实现了(杂)芳基醛/酮的直接、高选择性、高效且通用的还原胺化、醚化、酯化和膦化反应,这些反应极具挑战性或难以实现,仅使用二苯基亚磷酸酯[Ph2P(O)H]和无机碱即可实现。这些还原功能化能够模块化、结构和功能多样化地合成(杂)芳甲基叔胺、醚、酯、膦氧化物等,以及相关的农药、药物中间体、药品及其衍生物。与涉及加成、缩合和后续还原的经典羰基还原功能化相比,该策略通过Pudovik加成、膦-Brook重排和非常规亲核取代进行,代表了羰基还原功能化的一条未知途径(图1B)。
图片来源:Sci. Adv.
反应底物情况
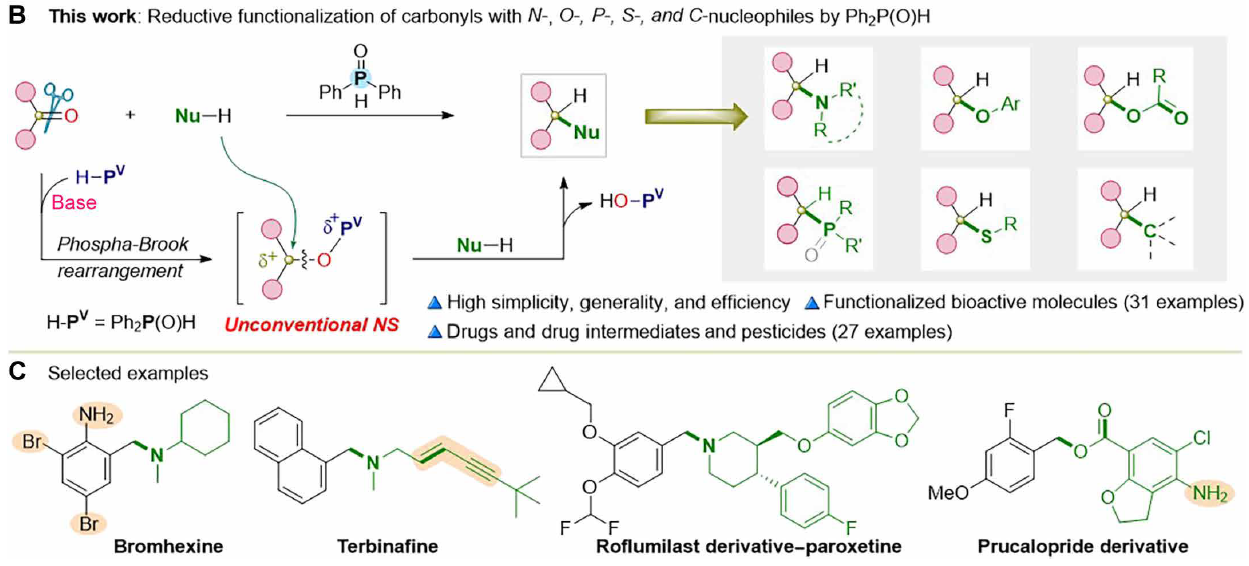
如图2所示,这种极其简单的方法允许从芳基醛/酮和仲胺直接且选择性地合成各种叔胺,产率高至极佳。带有各种电子富集和电子贫乏取代基的苯甲醛被发现是该反应的良好底物(1至13)。随后,进行了芳基醛与仲胺的正交反应,展示了仲胺的广泛底物范围,包括各种类型的开链(14至19)、环状(20至31)、杂环(32至39)和内环(40至43)骨架和官能团。官能团的良好兼容性通过它们在哌啶骨架中的存在得以突出,哌啶骨架是制药领域中最普遍的框架之一(33)。此外,仲磺酰胺也是羰基胺化反应的合适底物,生成复杂的叔磺酰胺(44至50),产率高。杂芳基醛也与仲胺顺利反应,生成所需的杂芳甲基叔胺(51至57)。此外,还获得了芳基酮的胺化产物(58和59)。值得注意的是,还实现了(杂)芳基二醛的直接二胺化(60至62),从而直接合成了潜在的三齿钳形配体(34)。不幸的是,由于无法通过[1,2]-膦-Brook重排形成关键中间体膦酸酯,脂肪族醛和酮不适用于这种还原胺化反应。
图片来源:Sci. Adv.
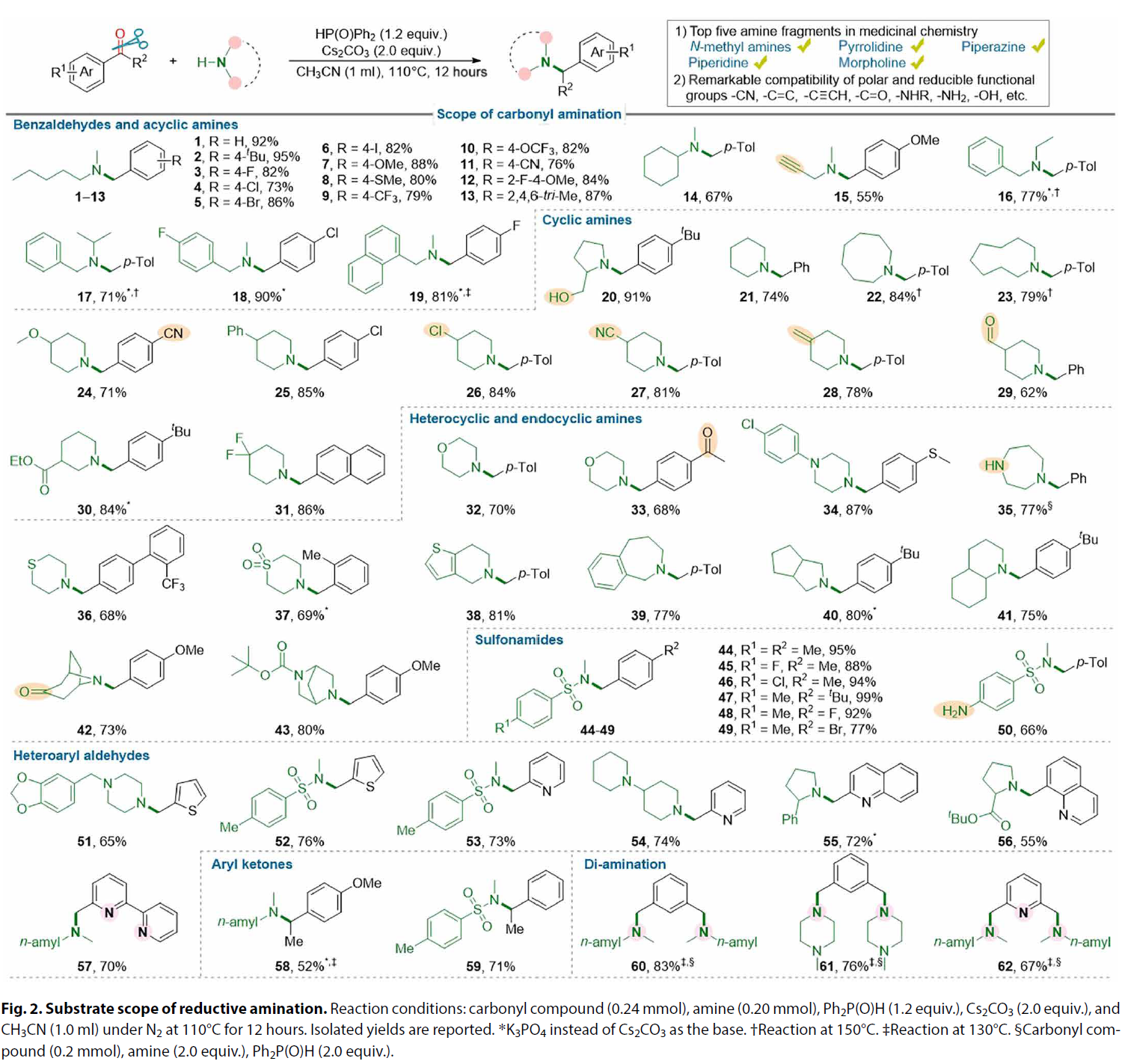
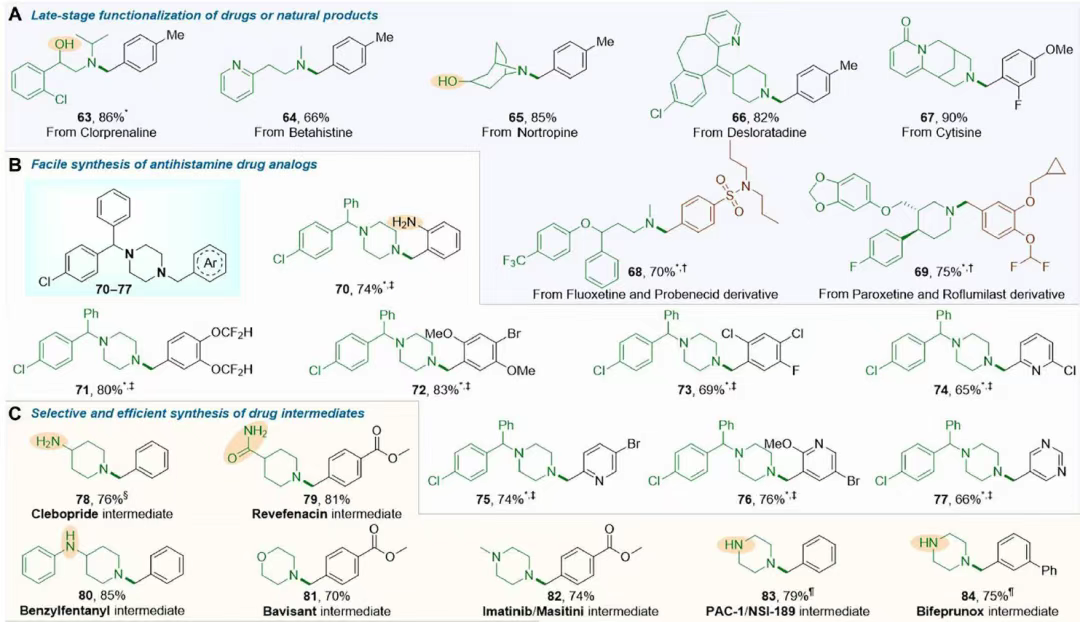
含有芳甲基和杂芳甲基单元的叔胺在药物中构成一个极其重要的骨架类别,在药物库中基于此类片段的条目超过200个。像克洛普雷林(63)、贝他司汀(64)、诺托品(65)、地氯雷他定(66)和金雀花碱(67)这样的药物很容易通过后期功能化形成基于芳甲基叔胺的药物衍生物。还获得了两种药物的组合衍生物,例如化合物68,由氟西汀和丙磺舒衍生而来,以及化合物69,由帕罗西汀和罗氟司特衍生而来(图3A),可能对多靶向药物具有潜在价值。此外,基于1-二芳甲基-4-(杂)芳甲基哌嗪骨架的一系列高度功能化的药物类似物(70至77),这些骨架在许多抗组胺药物中都有发现,通过各种功能化的(杂)芳基醛模块化构建(图3B)。此外,还可以选择性且高效地合成各种药物中间体(78至87),无论是否存在还原性和反应性官能团(图3C)。
图片来源:Sci. Adv.
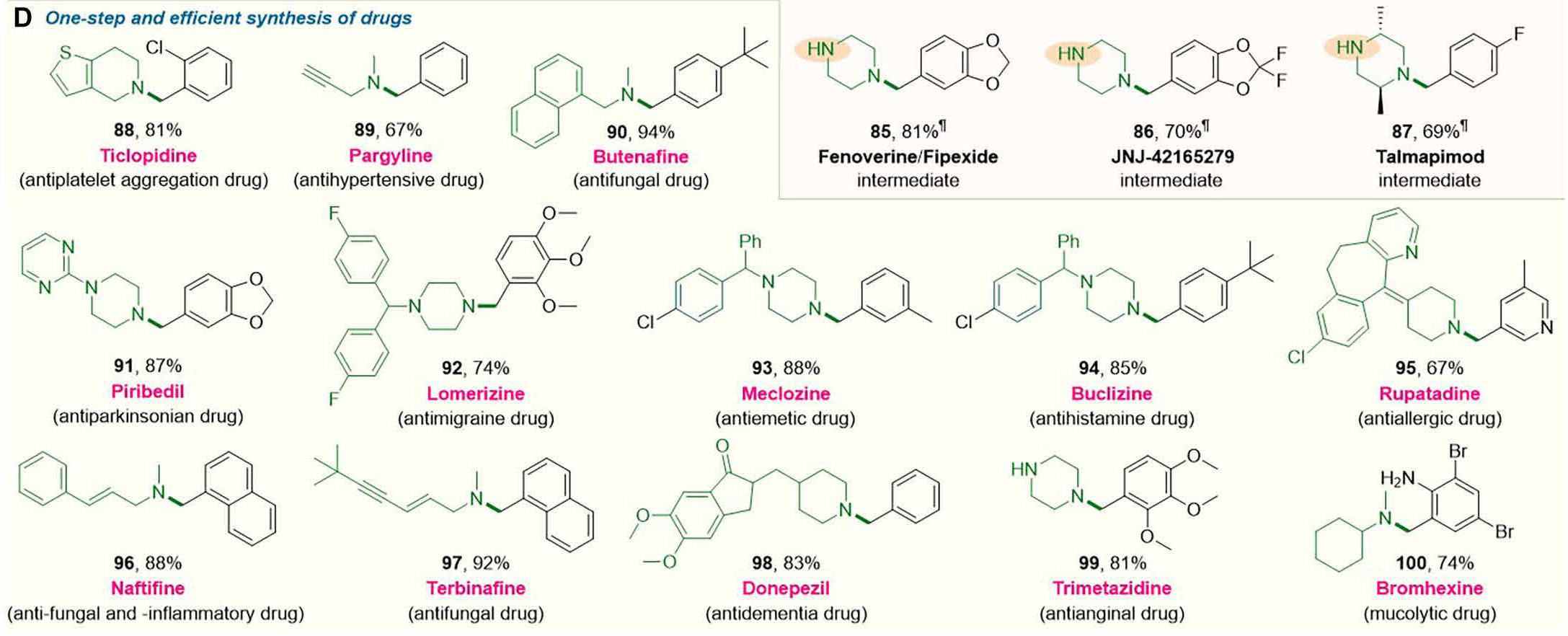
使用商业可用的原料成功直接制备了数十种药物,如氯吡格雷(88,81%)、帕吉林(89,67%)、布替萘芬(90,94%)、吡贝地尔(91,88%)、洛美利嗪(92,74%)、美克洛嗪(93,88%)、布克利嗪(94,85%)、鲁帕他定(95,67%)、那他芬(96,88%)、特比萘芬(97,92%)、多奈哌齐(98,83%)、曲美他嗪(99,81%)和溴己新(100,74%)(图3D)。
图片来源:Sci. Adv.
值得注意的是,传统上,这些药物和药物中间体及其衍生物的合成主要依赖于烷基卤化物的N-烷基化和过渡金属催化的偶联反应。有些情况需要繁琐的多步反应。例如,由于药物溴己新(100)在其苄基部分含有易受攻击的溴和初级芳基氨基基团,因此无法通过过渡金属催化的交叉偶联和N-烷基化直接合成;相反,它是通过低产率(<45%)的多步过程制备的(39)。与现有方法相比,这种简单的羰基胺化不仅能够在无过渡金属和有机卤化物的条件下合成这些药物和中间体,而且还能直接从易于获取的原料实现更高的产率和选择性。构建包含广泛结构单元和极性官能团的新且复杂的胺骨架是一个重大挑战,这通常是药物发现项目中的一个限制因素。除了对结构多样的胺底物的适用性外,这种羰基胺化在官能团耐受性和选择性方面也具有决定性优势。如图1和2所示,易在经典羰基还原胺化中发生反应的可还原基团,如末端炔基、氰基、末端烯基、N-Boc、脂肪族和芳香族酯,甚至脂肪族醛、脂肪族和芳香族酮羰基,都是可耐受的。此外,未保护的极性官能团,如初级和次级醇、初级和次级芳基氨基、初级烷基氨基和初级酰胺,也具有良好的兼容性。此外,由于更容易形成C─N双键(亚胺),比仲烷基氨基更具反应性的初级氨基被选择性地容纳。因此,这种还原功能化是传统胺化反应(如N-烷基化、过渡金属催化的交叉偶联和经典还原胺化)的极佳替代品,特别是在底物范围、极性官能团兼容性和化学选择性方面。因此,它具有巨大的潜力,能够合成具有多样化结构和功能特性的芳甲基和杂芳甲基叔胺,这些特性以前很难获得,从而推动药物发现工作。
羰基还原醚化和酯化
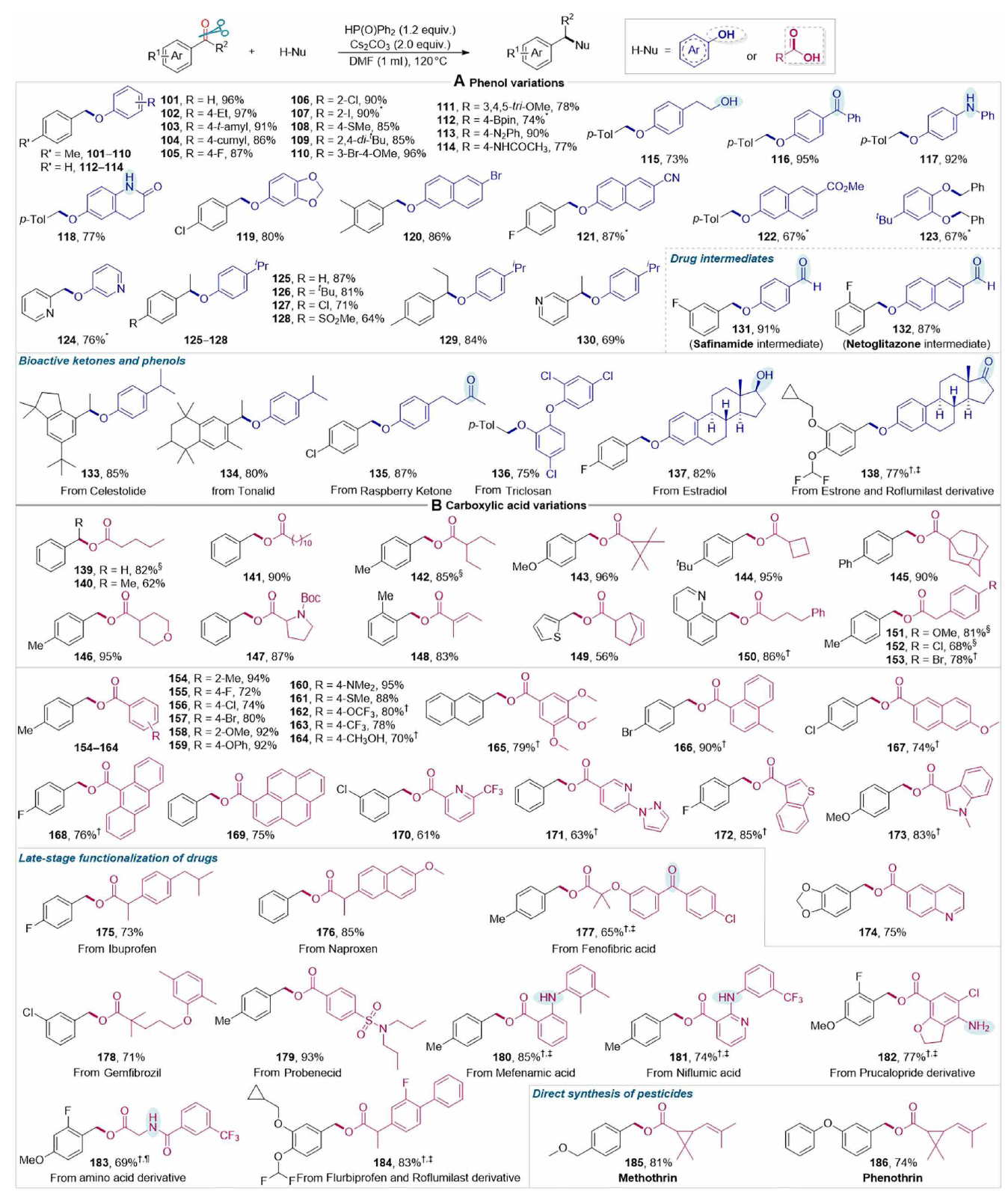
令人欣慰的是,这种还原功能化策略还能够通过处理(杂)芳基醛/酮与酚和羧酸,直接形成C─O单键,分别产生相应的非对称醚和酯,产率高。对于羰基还原醚化(图4A),包括取代酚(101至119)、萘酚(120至122)、儿茶酚(123)和杂芳基酚(124)在内的广泛酚类衍生物均能高效工作,以67至97%的产率提供结构和功能多样化的非对称(杂)芳醚。对于(杂)芳基酮(125至130),反应也能顺利进行,不会消除它们的α-H。含有反应性芳香醛羰基的酚底物经历了选择性和高效的醚化反应,分别产生了沙非酰胺(131)和netoglitazone(132)的中间体,同时保留了醛羰基。即使是更复杂的原料,如生物活性酮(celestolide,133;tonalid,134)和酚类衍生物(树莓酮,135;三氯生,136;雌二醇,137;雌酮,138)也被证明是可行的底物,以高产率提供了所需的后期功能化醚。值得注意的是,初级和次级醇(115和137),在还原醚化中具有反应性,也被选择性地耐受。类似地,(杂)芳基醛和酮与具有各种结构骨架的脂肪族羧酸的还原酯化反应,如线性(139至141)和支链(142)结构、三元和四元环(143和144)、笨重的金刚烷(145)和杂环(146和147),以及α,β-不饱和羧酸(148),也顺利进行(图4B)。该反应对各种苄基(151至153)、芳香(154至165)和多芳香(166至169)羧酸也有效。此外,杂芳族羧酸也是可行的底物(170至174)。显著的是,复杂药物分子和氨基酸衍生物(175至184)的后期功能化也容易进行,未保护的芳基初级(182)和次级(180和181)氨基基团不受影响,这些基团通常在传统酯化反应中不耐受。此外,这种酯化方法还能够直接合成农药甲氧普林(185,81%产率)和苯氧普林(186,74%产率),它们具有烯丙基基团和/或三元环。
图片来源:Sci. Adv.
醚和酯是制药、天然产物、农业化学品和功能材料中的重要结构单元(42–46)。由于醚化和酯化反应在化学中的基本性质,已有近两个世纪的发展,因此有无数的醚化和酯化方法。然而,传统醚化和酯化策略,如分子内脱水醚化/酯化和与烷基卤化物的O-烷基化,面临着化学选择性、底物范围和官能团兼容性方面的问题。这种策略使用醛和酮作为烷基化试剂,分别实现酚和羧酸的高选择性O-烷基化,在非常简单的条件下具有广泛的底物范围和显著的官能团耐受性。因此,这种直接O-烷基化提供了一种替代的醚化和酯化策略,能够轻松、绿色且骨架和取代基多样化的合成非对称醚和
羰基与仲膦氧化物的直接还原膦化反应
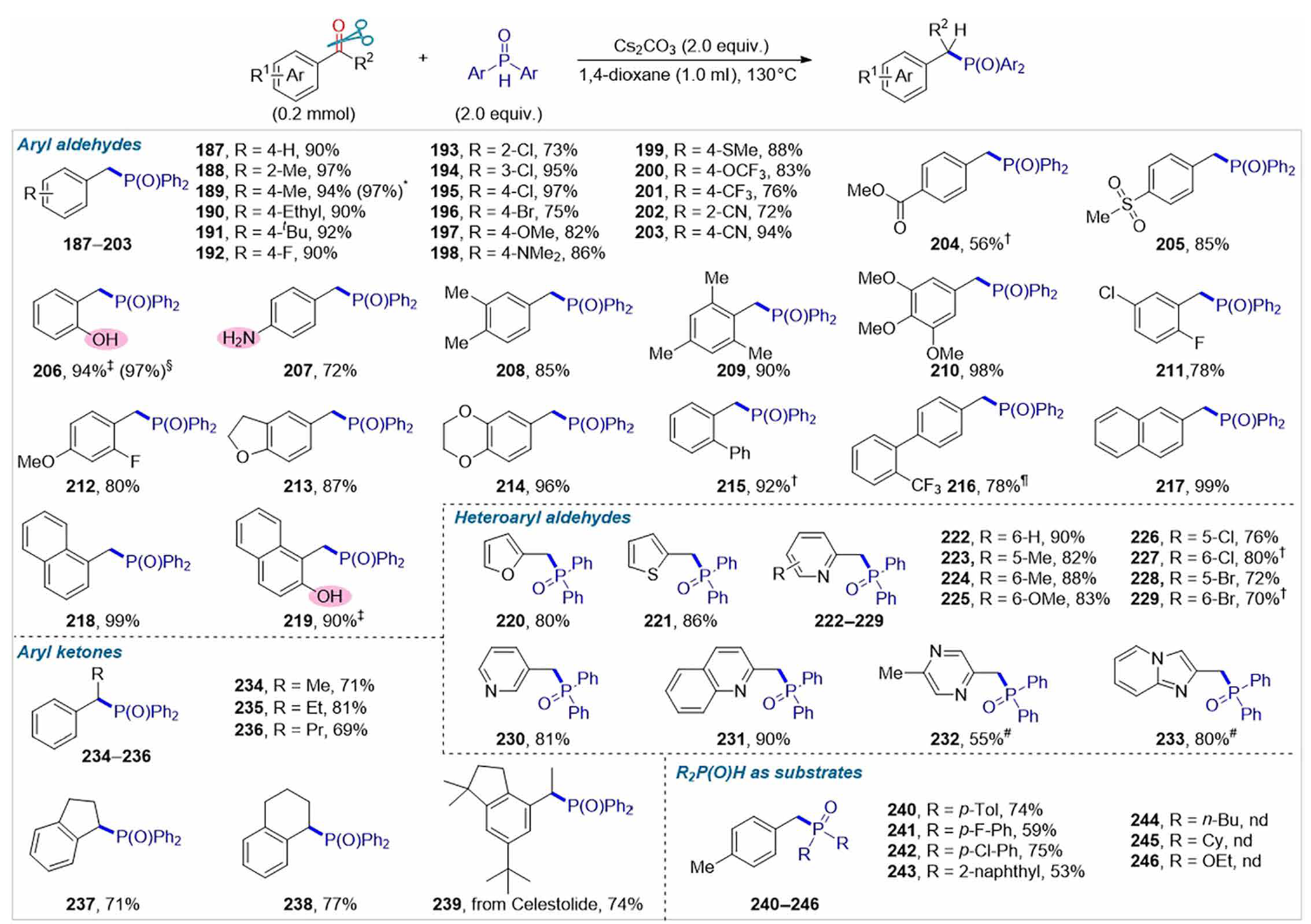
(杂)芳基醛与Ph2P(O)Hs顺利反应,生成芳甲基和杂芳甲基膦氧化物,产率高至极佳,对各种官能团具有显著的耐受性。芳基酮也被证明是可行的底物,提供了相应的α-取代苄基膦氧化物(234至239),产率为69至81%。值得注意的是,含有酚羟基(206和219)的芳香醛在上述还原醚化中是一个反应性基团,通过稍微调整反应条件表现良好。因此,2-羟基苄基二苯基膦氧化物(206),这是Denton(47)工作中的一种关键催化剂,通常在三步反应中以68%的产率在苛刻条件下制备,现在可以在5-毫米级反应中直接生产,结果更好(1.49克,97%)。
图片来源:Sci. Adv.
反应机理和扩展
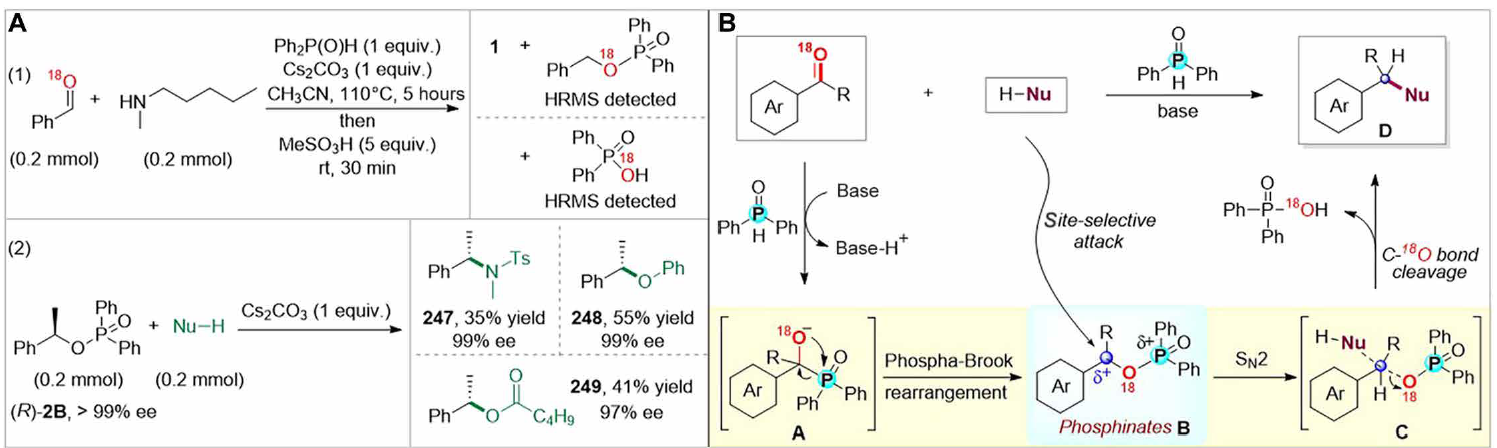
18O同位素标记实验表明,反应开始时(20分钟),观察到了一种[1,2]-膦-Brook型重排产物,即18O标记的膦酸酯(18O-1B),产率达到93%。该产物在其C─O─P单元的C原子上与N-甲基戊胺发生了选择性亲核取代反应,同时释放出18O标记的二苯基膦酸(Ph2P(O)18OH)作为副产物。随后,使用(R)-2B(99%对映体过量)与N-甲基-p-甲苯磺酰胺、苯酚和戊酸反应,分别得到了相应的手性化合物,即手性磺酰胺(247)、醚(248)和酯(249),其对映体过量值分别为99%、99%和97%。这些结果表明,该策略的关键步骤是通过SN2亲核取代反应进行的,通过扩展该策略,可能会开发出立体特异性的亲核取代反应。因此,提出了一个合理的反应机理(图6B)。最初,在碱的存在下形成了Ph2P(O)H阴离子,它对羰基进行亲核攻击,形成中间体A。中间体A迅速发生[1,2]-膦-Brook型重排,形成芳甲基膦酸酯B(31,49),该中间体被亲核试剂通过选择性C─O键断裂进行攻击,形成所需产物(D),同时释放出易于分离且具有商业价值的二苯基膦酸作为副产物。
图片来源:Sci. Adv.
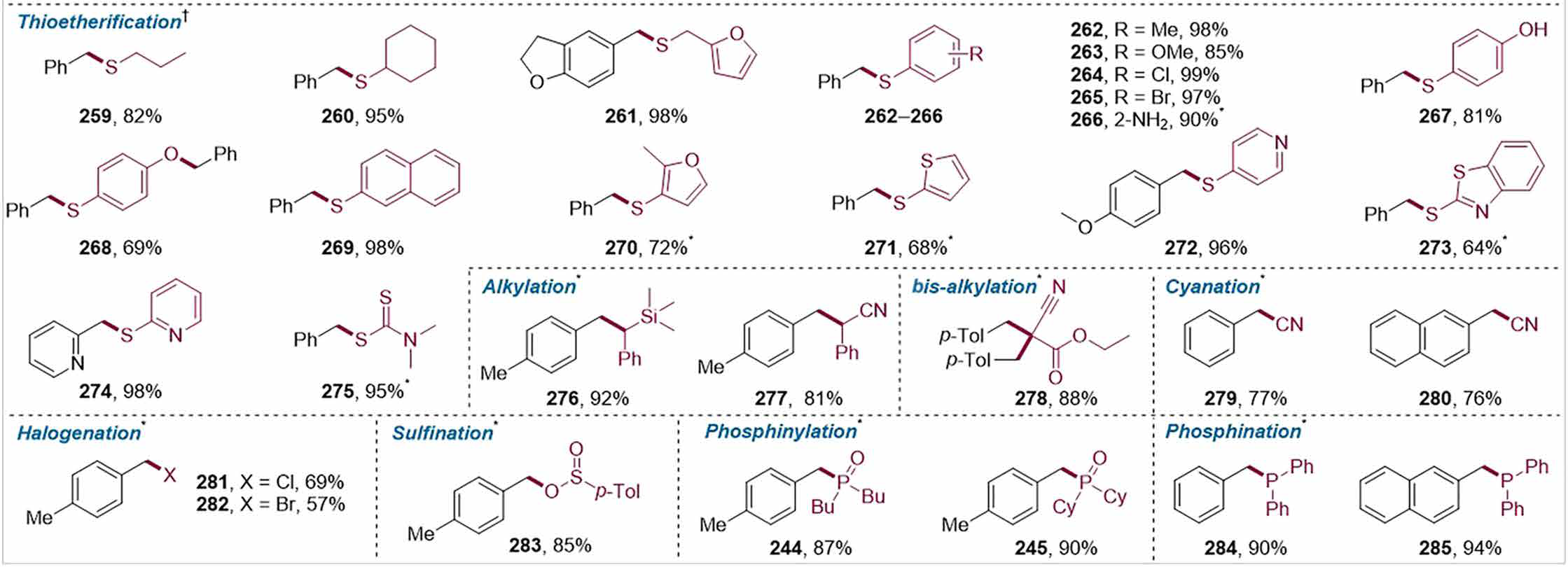
受该机理路径的启发,该策略成功扩展到其他化学键的直接和通用形成,如C─N(芳基)、C─S、C─C(sp3)、C─CN、C─X(Cl,Br)、C─OS(O)R和C─P(III)键(图6C)。通过使用其他亲核试剂,包括仲(杂)芳基胺、N-杂芳烃、S-亲核试剂、C-亲核试剂、三甲基硅基氰化物、乙基氰基乙酸酯、丁基锌卤化物和钠苯磺酸盐,分别实现了还原芳胺化(250至258)、硫醚化(259至275)、烷基化(276和277)、双烷基化(278)、氰化(279和280)、卤化(281和282)和磺化(283),分别得到了相应的产物,产率良好至极佳。使用其离子盐作为亲核试剂,也将二烷基膦氧化物纳入了相应的产物(244和245),产率高。令人高兴的是,该方法还扩展到了二苯基膦,允许通过还原膦化羰基直接产生三价磷化合物(284和285),产率极佳,这不仅避免了繁琐的多步合成,还消除了额外分离的需要。
图片来源:Sci. Adv.
总结
通过Ph2P(O)H实现的简单羰基还原功能化策略,允许直接构建多样的化学键,包括C─NR2、C─OAr、C─OC(O)R、C─P(O)R2、C─N(sp2C)、C─S、C─C(sp3)、C─CN、C─X (Cl,Br)、C─OS(O)R和C─P(III)键。已成功展示了其模块化、高效以及功能和结构多样化的合成为(杂)芳甲基叔胺、醚、酯、膦氧化物以及相关的农药、药物中间体、药品及其衍生物。该策略克服了传统羰基还原功能化、卤化物化学和过渡金属催化的交叉偶联的限制,特别是在底物范围、极性官能团兼容性和选择性方面,从而在还原功能化和醛/酮的磷介导转化领域以及基本反应领域,尤其是胺化、醚化和酯化方面取得了重要进展。
实验操作
胺类化合物通用合成方法 除特别说明外,所有反应均在氮气氛保护的手套箱中进行。取一个经烘箱干燥的25毫升施伦克管,装入磁力搅拌子,加入Cs2CO3(0.4 mmol, 2.0当量),随后依次加入Ph2P(O)H(0.24 mmol, 1.2当量)、羰基化合物(0.24 mmol, 1.2当量)、胺类化合物(0.20 mmol)及乙腈(1.0毫升)。反应体系在氮气保护下于110°C加热搅拌12小时。反应完成后将混合物冷却至室温,用饱和氯化铵水溶液(5.0毫升)洗涤,再用二氯甲烷萃取(3×5毫升)。合并有机相经无水硫酸钠干燥,真空浓缩后,通过硅胶(300-400目)柱层析[二氯甲烷/含2.0 M氨水的甲醇溶液=0.1%至10%梯度洗脱]分离得到目标胺化产物(1-100号)
免责声明:所载内容来源互联网,我们对文中观点保持中立,仅供参考,交流之目的。转载的稿件版权归原作者和机构所有,如有侵权,请联系我们删除。

