细胞和基因疗法临床试验的设计与交付!
概述
细胞和基因疗法(CAGT)在医学领域已取得显著进展,为遗传病患者提供了创新的治疗方案。最近,FDA批准了33种CAGT,其中有7种于去年才问世。在全球范围内,这一发展势头仍在持续,目前开展的相关试验多达2000余个,预计2024年将有50多款新产品上市。这些数据表明了CAGT对临床医疗具有重大影响,同时也意味着患者将有更多的CAGT领域治疗方案可选。
CAGT监管动态概览
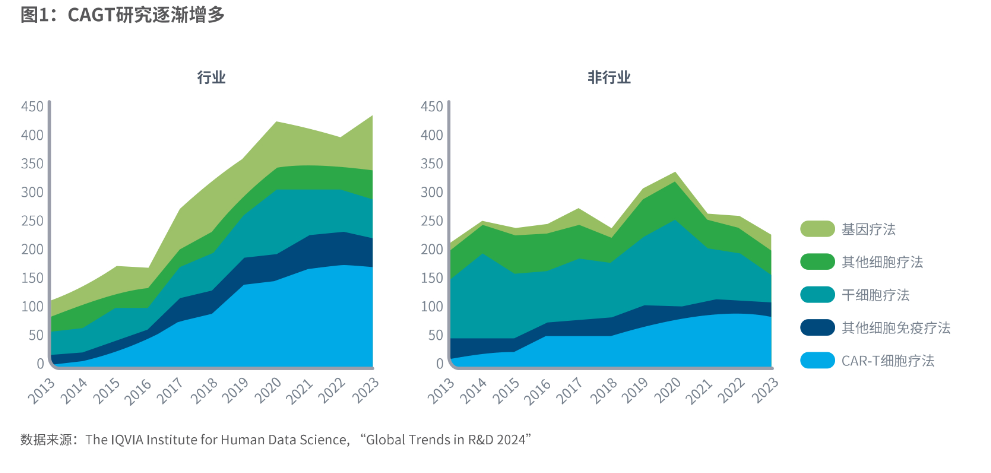
随着细胞和基因疗法创新的加速,监管环境也需要同步发展。图1表明了该领域研发创新的显著增长,随之也产生问题:监管部门、药物开发团队以及整个行业正在筹备哪些措施来应对这波创新浪潮?
监管机构正逐步适应并为CAGT的创新做好准备。其中FDA 的监管工作最为突出,特别是为生物制品评价和研究中心(CBER)所制定的指南。
 美国《处方药使用者费用法案》(PDUFA)为 FDA提供了招聘和培训人员、实施新流程和制定指南的工具,以支持下-波CAGT创新工作,借助各项资源助力CAGT研究。这种积极主动的方法清楚地表明了CAGT发展的动态性质,此举为未来五年内监管框架可能出现的重大变革奠定了基础。
美国《处方药使用者费用法案》(PDUFA)为 FDA提供了招聘和培训人员、实施新流程和制定指南的工具,以支持下-波CAGT创新工作,借助各项资源助力CAGT研究。这种积极主动的方法清楚地表明了CAGT发展的动态性质,此举为未来五年内监管框架可能出现的重大变革奠定了基础。
随着监管框架不断演变发展,申办方必须紧跟变化。此外,重要的是认识到FDA并非唯-一个正在塑造如此监管格局的机构。全球各地的监管机构正在通过WHO和ICH等平台开展合作,携手绘制CAGT监管工作的未来蓝图(图2)。这些国际合作对于营造具有凝聚力且可适应的监管环境而言至关重要,为CAGT创新格局提供了必要支持。
08前沿视点·VIEW POINT







免责声明:所载内容来源互联网,等公开渠道,我们对文中观点保持中立,仅供参考,交流之目的。转载的稿件版权归原作者和机构所有,如有侵权,请联系我们删除。

